
Sello de fibrina en la reparación de perforaciones timpánicas
RESUMEN
Antecedentes. En los últimos años se han efectuado diversas investigaciones sobre la utilización de adhesivos tisulares en otorrinolaringología. El uso de cianoacrilatos en la reparación de perforaciones timpánicas es controversial debido a los efectos tóxicos que pueden provocar en oído medio e interno. Asimismo, el uso creciente de derivados del fibrinógeno permite implementar nuevas opciones para la cirugía otológica. En el presente estudio, se presentan una investigación y una revisión sobre la elaboración de un sello de fibrina y papaína, fabricado con la infraestructura disponible en un hospital público para su uso en la reparación de perforaciones timpánicas en consultorio. Material y métodos. Se examinó a 35 pacientes con perforación timpánica de diferentes causas y con oído libre de otorrea. El material empleado para el cierre fue fascia homóloga de músculo temporal, con la adición del adhesivo antes mencionado. Se evaluaron los resultados en función del índice de cierre de la perforación y del tiempo de estancia del injerto sobre ésta. Resultados. En 31 (88.5%) pacientes se observó cierre de la perforación y en 20 (57.1%) fue necesario un segundo procedimiento para recolocar la fascia debido a migración del injerto. En algunos casos, aunque hubo migración del injerto, la perforación no se descubrió, o bien la permanencia de éste indujo reepitelización de la perforación, por lo que no hubo ya necesidad de recolocar la fascia (en tres pacientes). En 24 pacientes (70%) se observó mejoría auditiva luego del cierre de la perforación, y en el restante 30% no hubo cambios. La mayoría de los enfermos presentó migración de la fascia entre la segunda y la tercera semanas (> 60%). Conclusiones. La duración y la firmeza de la adhesión fueron suficientes para permitir, en condiciones adecuadas, el cierre de perforaciones timpánicas no marginales; en promedio, ello se logró después de la tercera semana. Palabras clave: adhesivos titulares, cianoacrilatos, perforación timpánica, fibrinógeno, sello de fibrina y papaína, injerto.
ABSTRACT
Background. In last years, diverse investigations have taken place on the use of tissue adhesives in otorhinolaryngology. The use of cianoacrylate in the repair of tympanic perforations is controversial due to the poisonous effects that can cause in middle and internal ear. Also, the increasing use of fibrinogen derivatives allows to implement new options for the otologic surgery. In this study, an investigation and a revision on the elaboration of a fibrin and papain seal are presented, made with the infrastructure available in a public hospital for its use in the repair of tympanic perforations in doctor’s office. Material and methods. It was examined 35 patients with tympanic perforation by different causes and free ear from otorrhea. The material used for the closing was homologous fascia of temporary muscle, plus the adhesive before mentioned. The results based on the index of perforation closing, and the graft stay time were evaluated on this one. Results. In 31 (88.5%) patient, perforation closing was observed, and in 20 (57.1%) it was necessary a second procedure to relocating fascia due migration of the graft. In some cases, although there was migration of the graft, the perforation was not discovered, or the permanence of the graft induced reepithelization of the perforation, reason why there was already no necessity to relocating fascia (in three patients). In 24 patients (70%) auditory improvement of the closing of the perforation was observed soon, and in 30% there were no changes. Most of patients displayed migration of fascia between the second and third weeks (> 60%). Conclusions. The duration and the firmness of the adhesion were sufficient to allow, in suitable conditions, the closing of nonmarginal tympanic perforations; in average, it was obtained after the third week.
Introducción
Antes de 1950, la cirugía de los procesos infecciosos crónicos del oído medio se limitaba principalmente a la extirpación de las lesiones irreversibles óseas y de partes blandas. Sus objetivos fundamentales estaban orientados a la erradicación de la lesión, pero no a la reconstrucción.1 Como se sabe, las perforaciones timpánicas pueden cerrarse de manera espontánea con o sin mejoría de la audición; ello es posible también con tratamiento médico o manejo quirúrgico (timpanoplastia).
Zöllner y Wullstein2 fueron los precursores de esta técnica y propusieron una clasificación de estos procedimientos basada en la ubicación del injerto respecto de los huesecillos del oído medio o las ventanas de la cóclea. Avances posteriores hicieron posible la combinación de una resección quirúrgica de las celdillas afectadas y una técnica de reconstrucción de la membrana timpánica y/o la cadena osicular. Con tal combinación, pudo restaurarse la función del oído medio. Las técnicas timpanoplásticas se han innovado, gracias a los adelantos en la tecnología microquirúrgica, con la implantación de prótesis osiculares y el uso de materiales homólogos.1
Para colocar el injerto sobre el remanente se han utilizado diversos materiales, por ejemplo películas absorbibles (gel film) de gelatina sintética, la cual es estéril y no antigénica. Esta película favorece una adhesión más firme del injerto sobre el remanente, lo que permite una reepitelización más fácil y de mayor calidad. Aun con ello, su adquisición se ve limitada dado su alto costo. La realización de miringoplastias tras la aplicación de diversas sustancias (incluidas nitrato de plata, ácido tricloroacético o ácido crómico) sobre el remanente timpánico era sumamente desagradable para la mucosa del oído medio. Así ocurría cuando estas sustancias no se aplicaban correctamente; además, todas ellas podrían ser ototóxicas para el oído interno si llegasen a penetrar éste a través de las ventanas cocleares. Hasta el momento, con el manejo de perforaciones timpánicas mediante las técnicas antes mencionadas se ha logrado un éxito de hasta 90%, lo cual se debe a que —en ocasiones— el injerto no se integra de manera adecuada, además de que son posibles otras complicaciones (por ejemplo, infección o mala técnica quirúrgica).3
Desarrollo de adhesivos para oído medio
Desde hace algunos años, se han llevado a cabo investigaciones sobre la utilización de adhesivos tisulares en áreas tales como ortopedia, trasplantes y cirugía maxilofacial, y más recientemente en el campo de la otorrinolaringología. Con dichos adhesivos puede lograrse una unión bioestable entre los tejidos, con lo que al mismo tiempo se favorecen los mecanismos de reparación tisular propios del paciente.
En 1890, Berger fue el primero en reportar el efecto hemostático de la fibrina. Posteriormente, en 1944, Kronkite y colaboradores utilizaron por primera vez fibrinógeno y trombina para reconstrucciones con injerto de piel. En 1972, Matras hizo lo mismo en animales de experimentación y en humanos respecto de la anastomosis de nervios, y en 1979 Staindl reportó el uso de este adhesivo en pacientes con hemorragia postamigdalectomía y tendencia hemorragípara.
Ya en 1983, Katzke y colaboradores4 reportaron el uso de adhesivos tisulares en otorrinolaringología y la ausencia, al utilizarlos, de efectos tóxicos en oído medio e interno. Luego de ello, Siedentop y colaboradores5, 6 aludieron a las características de adhesividad, hemostasia y reparación de heridas con el adhesivo tisular a base de fibrina; asimismo, establecieron que dicho material, colocado sobre la platina del estribo, es biocompatible y no causa efectos tóxicos.7 Strauss informó en 1984 que la tasa de perforación recurrente en timpanoplastias disminuía tras la utilización del adhesivo tisular a base de fibrina.8 Zikk (1990)9 y Wood, dos años antes (1988),10 comprobaron la ausencia de efectos tóxicos en oído medio e interno de chinchillas.
Desde hace dos décadas, se ha investigado el desarrollo de adhesivos tisulares útiles en cirugía de oído medio. En dicho desarrollo, ha sido importante determinar qué propiedades mecánicas, físicas y de biocompatibilidad son útiles en reconstrucciones de membrana timpánica, osiculoplastias, injertos nerviosos, o reparación de defectos que comuniquen a la fosa craneal.11, 12
Los procedimientos otológicos de índole quirúrgica implican, por lo regular, el uso de biomateriales o de tejidos biológicos, los cuales se utilizan en forma de injerto o de prótesis. Sin embargo, a pesar de que existe en el mercado una amplia variedad de materiales que el investigador clínico puede emplear, es permanente la búsqueda de materiales que reúnan ciertos requisitos básicos: eficacia, bajo costo, seguridad de que no provocarán efectos colaterales en el paciente y, si es posible, que su composición estructural sea lo más similar posible a la de los tejidos humanos.
Algunos materiales se han descartado en esta búsqueda debido a situaciones diversas: dificultad de obtención, eficacia insuficiente, control deficiente de sus componentes, entre otras. En muchos lugares, se les descarta debido al costo que representa el uso de materiales fabricados con tecnología de punta; en la mayoría de los casos, se requiere de un apoyo financiero sustancial para tener acceso a dichos materiales, además de que —luego de obtenerlos— debe también invertirse en distribuirlos y, lo que es más importante, en hacerlos accesibles a los pacientes.11, 12
Entre dichos materiales se encuentran los de tipo natural (como la fibrina y el colágeno) y los sintéticos (incluidos los derivados del cianoacrilato, el cual se emplea en un número importante de adhesivos comúnmente utilizados).
A diez años de que comenzaron a utilizarse los cianoacrilatos, los cuales desataron en un principio euforia, su uso disminuyó a partir de que Kerr y Smith encontraron, en investigaciones con gatos, que la aplicación de este tipo de materiales podía inducir una respuesta inflamatoria intensa en la mucosa del oído medio, y en algunos casos destrucción del hueso adyacente. Años después, Kauffman descubrió la misma respuesta en el oído humano pese a la utilización de esteroides. En el análisis de Kauffman, ello se debía a que los cianoacrilatos provocan angionecrosis, pérdida de tejido y reacción a cuerpo extraño. Además, las toxinas generadas pasaban al oído interno, con lo que se producía daño sensorial, lo cual impulsó el perfeccionamiento del material originalmente utilizado, hasta obtener el histoacrilato, empleado por igual en otras especialidades (como oftalmología y odontología) con mínimos efectos inflamatorios.13, 14 La FDA de EUA autorizó el uso intrahospitalario de este material, pero no se le usa en forma rutinaria dado su costo, especialmente alto, y de hecho en muchos hospitales no se cuenta con él.
Desde hace aproximadamente dos décadas, Siedentop y colaboradores15-17 realizaron estudios con derivados de la fibrina, material que ha mostrado en animales un destacado efecto adhesivo. Se han descrito diversas técnicas de preparación de fibrina, basadas en la utilización de sangre autóloga, pero hasta hace pocos años la FDA no había aprobado aún su uso, excepto en animales, debido a la posibilidad de transmisión del virus de la hepatitis (B y C) y del virus de inmunodeficiencia humana (VIH).
El equipo de Siedentop describió cinco métodos básicos para dicha preparación:
• Precipitación con etanol.
• Centrifugación como método único.
• Crioprecipitación; al respecto, se sabe que la conservación del adhesivo en medios a bajas temperaturas no afecta su eficacia, circunstancia que permite almacenar el producto hasta por cuatro semanas.
• Precipitación con etilenglicol o con sulfato de amonio.
• Utilización, en todos los procedimientos anteriores, de cloruro de calcio, técnica que permite la precipitación de una cantidad mayor de fibrinógeno.
Además del empleo de fibrina en solución como pegamento, se han desarrollado otros prototipos, entre los que se ubican los que forman una especie de gel que puede inyectarse directamente a la caja timpánica, utilizados sobre todo para la corrección de defectos de la duramadre, de dehiscencias de la pared ósea del seno lateral y de fístulas perilinfáticas.18 Los componentes principales de dichos prototipos son fibrinógeno y trombina. También se ha descubierto que el agregado de ciertas sustancias a la fibrina incrementa su poder adhesivo al degradar mayor cantidad de fibrinógeno. Al respecto, la papaína es una enzima proteolítica capaz de activar a varios cimógenos dentro del cuerpo humano, entre ellos los factores de coagulación y otras proteínas del tejido conectivo. De ello informó Zucker-Franklin en su estudio sobre la reparación de cartílago y la interrelación entre ésta y las plaquetas, la cual puede ser inducida por enzimas proteolíticas.19
Zubairov (1988) realizó nuevos experimentos sobre este aspecto y encontró que el adhesivo tisular acortaba la fase de cicatrización al aumentar los sitios de enlace para el factor X sobre la superficie del factor III; en ese caso, la actividad proteolítica de la papaína favorecía de manera importante el proceso.20 En México, Serrano reportó una investigación sobre adhesivo tisular a base de fibrina utilizado en timpanoplastia, y documentó un mejor sellado de las perforaciones sin efectos colaterales en humanos.21, 22
Relación entre fibrinógeno y papaína
La combinación del rico contenido de fibrinógeno precipitado por el cloruro de amonio, más el cloruro de calcio adicionado y otros factores de coagulación (entre ellos la trombina), ofrece un sustrato adecuado para que la adición de la papaína active al factor XIII de la coagulación, así como otros cimógenos contenidos en el plasma. De manera secundaria, la combinación genera entrecruzamiento de las cadenas alfa del fibrinógeno, lo cual favorece la formación de una red de fibrina con un efecto adhesivo importante. La fibrina producida se adhiere a los tejidos expuestos tras la lesión tisular, con especial afinidad hacia las fibras de colágeno. La malla de fibrina formada sirve como soporte para la proliferación de fibroblastos y capilares que se producen en el proceso de cicatrización. Este mecanismo depende de muchos factores (entre ellos, trombina, fibrina y factor XIII) que estimulan la proliferación de fibroblastos.
Minutos después de combinar los componentes del adhesivo, 70% del fibrinógeno se transforma en fibrina (Figura 1). La aplicación del adhesivo ofrece una matriz sobre la que dan inicio los fenómenos de regeneración para permitir que el tejido subyacente inicie en forma natural los procesos de unión tisular.
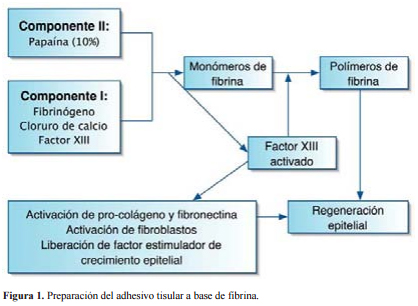
La principal dificultad para la obtención de los adhesivos citados es la obtención de una cantidad suficiente de fibrinógeno concentrado, el cual es el componente más variable del adhesivo, aunque también del que depende su capacidad de unión. En el mercado existen adhesivos que combinan la acción del fibrinógeno con la de la trombina (Tissucol™ Baxter); son bastante efectivos, pero caros, además de que el volumen envasado es pequeño (por ejemplo, el envase de Tissucol™ Baxter contiene sólo entre 1 y 3 mL de adhesivo).
Dinámica de regeneración de la membrana timpánica
Deben destacarse los mecanismos de migración de injertos de membrana timpánica que, en parte, explican algunas fallas en la colocación de injertos al interactuar con los mecanismos naturales que ocurren en la membrana. Son cuatro las teorías mediante las que se pretende explicar dichas fallas: teoría del flujo linfático, teoría de vibración, teoría de movimientos ameboideos y teoría de crecimiento diferencial en el centro. Esta última alternativa es la más aceptada; de acuerdo con ella, la migración se debe a la importante actividad mitótica en el centro de una estructura en la que el patrón de crecimiento es del centro a la periferia (es decir, en forma centrípeta al centro de generación celular).
En el caso de la membrana timpánica, se han realizado estudios como el de Del Ángel en el Hospital Juárez de México.23 En este estudio, se encontró que los injertos de membrana de fascia de músculo temporal, colocados sobre la membrana timpánica íntegra o perforada, tienden a emigrar hacia arriba y hacia atrás. Ello explicaría ciertos casos de falla de injerto, pero no por aplicación inadecuada de la técnica, sino como resultado del crecimiento centrípeto. En función de esto último, podría pensarse que el uso de sustancias que favorecerían una adhesividad rápida y efectiva podría evitar que el injerto migrase a otra región, en vista de que se ha adherido a la superficie de la membrana.
Hasta el momento, con el manejo de perforaciones timpánicas mediante las técnicas mencionadas se ha logrado un éxito de hasta 90%, debido a que en ocasiones el injerto no se integra de manera adecuada, además de otras posibles complicaciones (como infección o técnica quirúrgica inadecuada).3
Uno de los principales motivos de consulta es la otitis media crónica, la cual —de manera casi constante y como parte de la evolución natural de la enfermedad— ocasiona perforaciones timpánicas. Asimismo, es frecuente la consulta de pacientes que cursan con perforaciones timpánicas causadas por mecanismos diferentes del infeccioso, generalmente postraumáticas. Tras examinar al paciente, y después de eliminar cualquier posibilidad de infección y evaluar el estado de la mucosa de la caja timpánica y la capacidad de audición, el manejo quirúrgico de estas perforaciones con reconstrucción osicular puede ofrecer al paciente una solución real para su problema. Sin embargo, la gran cantidad de pacientes atendidos en las instituciones de salud pública del país, además de la falta de tiempos quirúrgicos suficientes, significan un estímulo para la búsqueda de nuevas alternativas quirúrgicas que brinden mejores resultados al enfermo, y que al mismo tiempo disminuyan el número de fracasos y, con ello, los costos por atención y la sobresaturación de los turnos quirúrgicos.
De hecho, el uso de adhesivos comerciales involucra gastos importantes debido a su alto costo, lo cual limita su uso a una pequeña parte de la población enferma, es decir aquella que puede hacer frente a los gastos inherentes; a ello, deben agregarse los gastos relacionados con el proceso de hospitalización y el manejo postoperatorio. Ante tal situación, la posibilidad de producir el adhesivo tisular con los recursos con los que cuente el hospital, bajo la supervisión adecuada del laboratorio, ofrece una alternativa para mejorar las técnicas utilizadas. Además, debe destacarse que, con el uso del citado adhesivo tisular, hasta el momento no se han detectado efectos adversos en oído, con la ventaja de que este tipo de adhesivo favorece una rápida cicatrización.
Objetivos
1. Utilización, en el consultorio, del adhesivo tisular a base de fibrina para el manejo de perforaciones timpánicas.
2. Determinación del tiempo promedio de estancia del injerto sobre la perforación al utilizar sello de fibrina.
Material y métodos
Se realizó un estudio prospectivo, longitudinal y observacional cuyo universo estuvo conformado por pacientes que acudieron a consulta en el Servicio de Otorrinolaringología y Cirugía de Cabeza y Cuello del Hospital Juárez de México con diagnóstico de perforación timpánica, en forma independiente de la causa de ésta (postraumática, otitis media crónica, dehiscencia de injerto colocado en quirófano).
Tras cerciorarse de que los probables participantes en el estudio cumplían con los criterios de inclusión, se explicó a cada uno de ellos el procedimiento, los riesgos de éste y el seguimiento que debían mantener después de la intervención. Todo procedimiento fue autorizado mediante consentimiento informado escrito.
Criterios de inclusión
1. Pacientes con perforación timpánica central de 30 a 60% y presencia de remanente timpánico.
2. Edad: mayores de 15 años.
3. Sexo: indistinto.
4. Cavidad de oído medio: libre de secreción durante por lo menos seis semanas antes del procedimiento.
5. Tomografía computarizada de oídos: ausencia de enfermedad en oído medio (por ejemplo, colesteatoma).
6. Capacidad de audición: no se tomó en cuenta, puesto que en varios casos el objetivo no fue la mejora de la audición, sino la corrección de la perforación timpánica.
Criterios de exclusión
1. Pacientes con perforaciones marginales.
2. Presencia de proceso infeccioso activo en oído medio, o de colesteatoma, así como de infección de vías respiratorias superiores.
3. Datos sugerentes de colesteatoma en la tomografía computarizada de oídos.
4. Pacientes que explícitamente no cumplieron con alguno de los criterios de inclusión antes mencionados.
Métodos
Luego de reunir la muestra, se realizó una exploración otorrinolaringológica completa en el momento de la colocación del injerto para comprobar ausencia de infección. Bajo visión microscópica, se determinaron el tamaño y las características de la perforación. Posteriormente se preparó el fragmento de fascia homóloga de músculo temporal, obtenido en condiciones esté- riles de otros pacientes sometidos previamente a cirugía otológica. La fascia utilizada tenía, como máximo, dos semanas de haberse extraído. Se recortaron fragmentos lo suficientemente grandes para evitar que, durante la migración, se descubriera de nuevo la perforación.
Se impregnó el remanente con adhesivo tisular preparado en el hospital (véase, después, la técnica de preparación), y sobre él se colocó el fragmento de fascia para —a continuación— acomodarlo en forma tal que cubriera perfectamente la perforación; el paso final consistió en aplicar una gota de adhesivo sobre el injerto ya colocado.
Se indicaron a los pacientes cuidados de oído perforado, y se les citó para revisión en consulta externa una semana después del procedimiento, y también a las semanas 2, 3, 4 y 6.
La presentación de los resultados se hizo mediante gráficas y tablas descriptivas.
Técnica de preparación del adhesivo tisular
La técnica de preparación del adhesivo tisular se basó en la diseñada por Sandoval21 en 1991 y se realizó en las instalaciones del Banco de Sangre del Hospital Juárez de México, contando con los recursos de esta institución, bajo la supervisión del QBP Conrado Medina.
El adhesivo se compone de dos partes:
• Componente I: diseñado a base de fibrinógeno, factor XIII (F XIII) y cloruro de calcio (ClCa2 ).
• Componente II: papaína a 10%.
Para obtener el componente I, se seleccionaron las unidades de sangre total de los pacientes candidatos a donación en el Banco de Sangre; a ésta se le agregaron 4 cc de solución de citrato-fosfato-dextrosa-adenina (CPDA) + adenina, dextrosa, sorbitol, cloruro de sodio y manitol (ADSOL, del inglés adenine, dextrose, sorbitol, sodium chloride and mannitol). A continuación, se efectuó el fraccionamiento en componentes para extraer el plasma fresco (rico en factores de coagulación) y someterlo a congelamiento. Posteriormente, el plasma fresco se sometió a pruebas de detección de VIH, y antígenos contra sífilis, hepatitis B y hepatitis C
Tras obtener las pruebas de certificación, de la unidad de plasma se realizó una colección en cuatro tubos estériles, para centrifugar a 3 200 RPM durante 12 minutos. Se tomaron 10 cc del plasma centrifugado y se le colocó en cuatro diferentes tubos plásticos estériles, con 1.3 cc de solución estéril, fría, y saturada de sulfato de amonio purificado agregado a cada tubo. Con lo anterior, el fibrinógeno se precipitaba de inmediato. Más tarde, se procedió a decantar el sobrenadante para congelarlo a – 25 °C en tubos estériles hasta su uso.
Finalmente, el fibrinógeno se diluyó en 1 cc de solución de ClCa2 en el momento en que se le utilizó, y de esta manera se obtuvo el componente I; luego de obtenerlo, se le conservó en refrigeración.
El componente II se integró al mezclar 1 g de papaína en solución de agua bidestilada en relación 1:10 (Laboratorios REAMEX, número de catálogo P3125). La forma de presentación fue en suspensión en 0.05 M de acetato de sodio (pH: 4.5).
Para la obtención final del adhesivo se mezclaron en partes iguales ambos componentes justo en el momento de utilizárseles (Figura 1).
Resultados
Se reunió una muestra de 35 pacientes con perforación timpánica que cubrían los criterios de inclusión ya citados: ocho hombres (22.8% de la muestra) y 27 mujeres (77.2%). Sus edades oscilaban entre 16 y 60 años con un promedio de 34.2 años. Prácticamente todos los pacientes refirieron oído libre de secreción durante por lo menos tres meses antes de la aplicación del injerto. Las causas que originaron la perforación se muestran en la tabla 1.

En cuanto a su ubicación, las perforaciones centrales predominaron en el estudio (57%); el tamaño de la perforación fue en su mayoría de entre 30 y 50% de la membrana. Los resultados completos se muestran en las tablas 2 y 3.

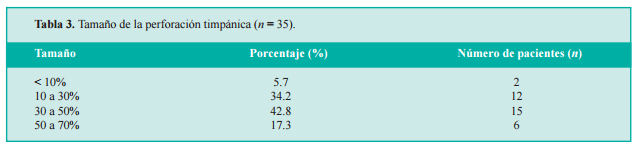
De los 35 pacientes, en 31 (88.5%) cerró la perforación para mantenerse cerrada después de la sexta semana de revisión.
Como se sabe, cualquier cuerpo colocado sobre la superficie de la membrana timpánica (o de su remanente) experimenta un fenómeno de migración; el caso de los injertos de fascia no constituye una excepción: 32 (91.4%) participantes experimentaron migración. En algunos, esta migración provocó que la perforación se descubriera, por lo que fue necesario colocar una nueva fascia en un segundo tiempo en 20 participantes (57.1%). En algunos casos, aunque hubo migración, la perforación no se descubrió, o bien la permanencia del injerto logró que reepitelizara la perforación, con lo que no hubo ya necesidad de recolocación de la fascia.
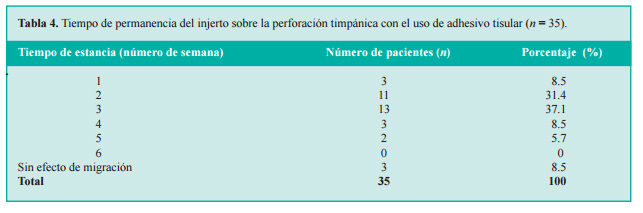
En la tabla 4 se muestran los resultados referentes a la permanencia del injerto sobre la perforación timpánica y, por ende, al tiempo que tardaron en migrar del sitio original de implantación. Estas valoraciones se realizaron en las visitas periódicas.
En 31 (89%) pacientes se logró el cierre de la perforación. En otros cuatro (11%), ello no fue posible. De estos últimos, en dos casos la ausencia de cierre se debió a migración de la fascia desde la primera semana: en un tercer paciente, el cierre fue obstaculizado por rinitis alérgica, y en el último por infección de vías respiratorias superiores y cuadro de otitis secundaria con secreción.
Del total de pacientes, 24 (70%) reportaron mejoría de la audición luego de conseguir el cierre de la perforación; el restante 30% no mostró cambios, y ningún paciente experimentó empeoramiento de la audición después de la aplicación del injerto.
Durante la realización del estudio, seis pacientes desarrollaron secreción de oído medio, incluidos tres de aquellos en los que se frustró el injerto. En los seis se procedió a uso de gotas óticas de ciprofloxacino, más ciprofloxacino por vía oral. Una vez controlada la infección, y aproximadamente después de seis semanas, se reintentó la colocación del injerto, pero sólo en tres (50%) se obtuvo el cierre. De los tres restantes, uno era el que padecía rinitis alérgica (en éste, no se logró el cierre), y en los otros dos sólo se desarrolló un recubrimiento epitelial parcial.
No se observaron efectos adversos tras la aplicación del adhesivo (reacción a cuerpo extraño, dermatitis o alguna forma de celulitis).
Discusión
En los últimos 15 años, los adhesivos a base de fibrina han experimentado un desarrollo notable, y con las nuevas técnicas de manufactura la calidad del producto es excelente: aun así, estas circunstancias son, precisamente, las que han generado un incremento sustancial (directamente proporcional) de los costos. En todo el mundo, estos adhesivos se utilizan en otorrinolaringología para reparación del nervio facial, osiculoplastia y procedimientos timpanoplásticos, corrección de fístula de líquido cefalorraquídeo, reconstrucciones de la pared posterior del conducto, sellado de fístulas perilinfáticas y obliteración del seno frontal y de las grandes cavidades de mastoidectomía (combinando, en este último caso, con paté de hueso).24
Dado que este tipo de adhesivos se prepara con hemoderivados, hasta hace pocos años su uso estaba limitado ante el riesgo de contagio por VIH y los virus de la hepatitis B y C. Actualmente —gracias al exigente control de calidad que se sigue al elaborarlos—, en EUA la FDA ha autorizado su uso.
Los estudios básicos sobre preparación de adhesivos a base de fibrina se deben a Siedentop y colaboradores;5-7 en los casos reportados por estos autores, la adición de diversas sustancias precipita el fibrinógeno. El presente estudio tomó como base los resultados obtenidos por Sandoval,21 quien utilizó una formula muy similar a la aquí empleada (también a base de fibrinógeno y papaína) para reparar perforaciones timpánicas. Las presentaciones comerciales de este tipo de adhesivos por lo general son combinaciones con derivados de la trombina; también ofrecen excelentes resultados, pero son más caros debido a la infraestructura requerida para obtener los dos componentes necesarios. La papaína tiene la ventaja de ser relativamente barata, además de que está lista para usarse desde el momento en que se le adquiere en forma de suspensión. Además, los adhesivos hechos a base de fibrina son más ventajosos que los de cianoacrilato dada su naturaleza biodegradable.
Los adhesivos autólogos tienen la ventaja de ser prácticamente inofensivos para los usuarios, ya que se preparan a partir de su propia sangre. En este estudio, se utilizó sangre tipo O Rh positivo (considerada para donación universal). Esta sangre fue sometida al más estricto control para descartar cualquier posibilidad de infección. De hecho, ninguno de los participantes en el estudio desarrolló alguna reacción considerada “tóxica”. En la literatura, no se reporta en absoluto sobre este particular. Por el contrario, la toxicidad puede presentarse al utilizar adhesivos fabricados industrialmente, aspecto sobre el cual sí existen descripciones en la literatura.
El adhesivo utilizado en el presente trabajo es de fácil preparación: tan sólo se requiere de un par de minutos para mezclar los componentes, ya que éstos se someten a preparación previa; el fibrinógeno precipitado puede conservarse en refrigeración hasta por cuatro meses sin degradación de su calidad. La papaína, por su parte, se utilizó en suspensión y se le diluyó para obtenerla en una concentración de 10%. También se le mantuvo en refrigeración —conforme con las especificaciones del laboratorio—, con lo que se conservó su poder enzimático. La preparación de papaína puede realizarse justo en el momento de utilizarla, sin necesidad de efectuar todo el procedimiento de separación de los componentes de la sangre para su posterior reconstitución junto con los otros compuestos que integran la fórmula. En total, la preparación del componente I duró dos días, dado que era necesario esperar los resultados que descartaran toda posibilidad de infección.
Con excepción del multicitado estudio de Sandoval,21 en la revisión de la literatura no se encontró algún otro estudio similar sobre cierre de perforación con adhesivo. En el trabajo de Sandoval, en 72.5% de la muestra se logró el cierre de la perforación timpánica con un adhesivo similar al aquí empleado. Con algunos cambios en la concentración de sulfato de amonio y cloruro de calcio respecto de la preparación de Sandoval, en el presente trabajo se logró cierre de perforaciones en hasta 88% de las intervenciones aplicadas. Ciertamente, Siedentop y colaboradores publicaron un estudio en el que mencionan el uso de este adhesivo (precipitando el fibrinógeno con sulfato de amonio); en ese trabajo, en diez casos de miringoplastia se observó cierre de la perforación. Empero, en dicho estudio no se especifica la evolución en el tiempo de los pacientes examinados.16
En el estudio realizado por Del Ángel, 23 se examinaron los patrones de migración sobre la superficie de la membrana timpánica (100% de la muestra de Del Ángel presentó el fenómeno de migración cerca de la segunda semana después de la colocación de la fascia).
Al examinar de nuevo la tabla 4, queda claro, en la sección de resultados de este estudio, que 31.4% de los pacientes presentó migración en la segunda semana, y que el porcentaje mayor de individuos (37% de la muestra) que iniciaron migración del injerto se observó hasta la tercera semana. Incluso, en dos pacientes la migración ocurrió hasta la tercera semana, y en tres no hubo migración. De ahí la ventaja de utilizar el adhesivo, puesto que su permanencia por mayor tiempo sobre la perforación disminuye el fenómeno de migración y permite una reepitelización más adecuada; al respecto, en tres pacientes (8.5%) no se observó migración.
En algunos casos, fue necesario recolocar el injerto. Sin embargo, en varios pacientes —después de iniciado el patrón de migración— se detectaron fenómenos de regeneración de la membrana timpánica y, por ende, no fue ya necesario recolocar el injerto de fascia.
En el estudio de Sandoval se registraron complicaciones tales como otorrea después de la colocación del injerto en 27.5%,21 pero no se mencionan las causas ni se indican las modalidades de seguimiento de los pacientes. En el presente estudio, en seis casos (15%) se observó otorrea. De éstos, en dos casos se justificó la infección: uno por exacerbación de rinitis alérgica, y otro por infección de vías respiratorias superiores.
Conclusiones
1. El sello a base de fibrina, obtenido de fascia homóloga del músculo temporal, puede prepararse con facilidad y en forma rápida, incluso justo en el momento de utilizársele. Representa una alternativa práctica a los productos comerciales, caros y en ocasiones difíciles de conseguir en países como México.
2. La duración y la firmeza de la adhesión son suficientes para permitir, en condiciones adecuadas, la unión del injerto a las perforaciones timpánicas no marginales que cuenten con remanente suficiente para sostener éste. En promedio, esto se logra después de la tercera semana.
3. El uso en el consultorio de adhesivo tisular para la reparación de perforaciones brinda un mejor resultado que las intervenciones sin adhesivo.
4. Este estudio mostró que es posible preparar el adhesivo con recursos como aquellos de los que se dispone en casi todos los hospitales, ya que la preparación del biomaterial sólo requiere de una Unidad de Sangre. De lograr esto, se obtendrá un producto útil, de rápida y fácil preparación, con bajo costo, que permitirá la realización de diversos procedimientos quirúrgicos en oído.
Referencias
1. Goodhill V, Brockman S, Harris H, et al. Cirugía de la otomastoiditis: mastoidectomía y timpanoplastia. En: Goodhill V. El oído. Salvat, Barcelona, 1993; pp. 362-85.
2. Wullstein H. Theory and practice of tympanoplasty. Laryngoscope 1956; 66: 1076-93.
3. Lambert PR, Mc Elveen JT. Tympanoplastic surgery for chronic ear disease. En: Cummings CW, Gates GA. Otolaringology. Head and neck surgery. Mosby, St. Louis, 3rd. ed., 1998; pp. 3108-17.
4. Katzke D, Pusalkar A, Steinbach E. The effect of fibrin tissue adhesive in middle ear. J Laryngol Otol 1983; 97 (2): 141-7.
5. Siedentop KH, Harris DM, Loewy A. Experimental use of fibrin tissue adhesive in middle ear surgery. Laryngoscope 1983; 93: 1310-3.
6. Siedentop KH, Harris DM, Sanchez B. Autologous fibrin tissue adhesive. Laryngoscope 1985; 95: 1074-6.
7. Siedentop KH, Harris DM, Sanchez B. Autologous fibrin tissue adhesive: factors influencing bonding power. Laryngoscope 1988; 98 (7): 731-3.
8. Strauss P, Pult P, Kurzeja A, et al. Does human fibrinogen glue improve results in tympanoplasty? Laryngol Rhinol Otol (Stuttg) 1984; 63 (12): 615-7.
9. Zikk D, Rapapport Y, Himerlfarb MZ. Changes in auditory function associated with 2-cyano-butyl-acrylate adhesive implanted en the middle ear of experimental animals. Laryngoscope 1990; 100: 179-83.
10. Wood AP, Harner SG. The effect of fibrin tissue adhesive in middle ear in chinchillas. Otoloaryngol Head Neck Surg 1988; 98 (2):104-10.
11.Li JC, Leonetti JP, Mokarry V. The concept of transtympanic injection of fibrin Caulk. Arch Otolaryngol Head Neck Surg 1993; 119: 854-7.
12. Hadlock T, Elisseeff J, Langer R, et al. A tissueengineered conduit for peripheral nerve repair. Arch Otolaryngol Head Neck Surg 1998; 124: 1081-6.
13. Brown PN, McGuff HS, Noorily AD. Comparison of Noctylcyanoacrylate vs suture in the stabilization of cartilage grafts. Arch Otolaryngol Head Neck Surg 1996; 122 (8): 873-7.
14. Toriumi DM, Raslan M, Tardy ME. Histotoxicity of cyanoacrylate tissue adhesives. A comparative study. Arch Otolaringol Head Neck Surg 1990; 116 (5): 546-50.
15. Siedentop KH, Harris DM, Ham KR. Extended experimental and preliminary surgical findings with autologous fibrin tissue adhesive made from patient’s own blood. Laryngoscope 1986; 96: 1062-4.
16. Siedentop KH, Park JJ, Sanchez B. An autologous fibrin tissue adhesive with greater bonding power. Arch Otolaringol Head Neck Surg 1995; 121 (7): 769-72.
17. Siedentop KH, Chung SE, Park JJ, et al. Evaluation of pooled fibrin sealant for ear surgery. AM J Otol 1997;
18: 660-4. 18. Vanclooster C, Debruyne F, Vantrappen G, et al. Labyrinthine fistulae: a retrospective analysis. Acta Othorinolaryngol Belg 1997; 51 (2): 119-21.
19. Zucker-Franklin D, Rosenberg L. Platelet interaction with modified articular cartilage, its possible relevance to joint repare. J Clin Invest 1977; 54 (4): 641-51.
20. Zubairov DM, Timeraev VA, Kisslev VA, Kirshin SV. Interaction of human prothrombin with tissue thromboplastin. Biokhinia 1984; 54 (6): 1046-54.
21. Sandoval SJ. Adhesivo tisular FP en el manejo de perforaciones timpánicas.México, IMSS, 1991. 22. Rapaport SI. Introducción a la hepatología. Salvat, México, 2a. ed., 1994.
23. Del Ángel LMC. Patrones de migración de fascia temporal en membrana íntegra y perforada. Reporte de tesis, Hospital Juárez de México, SS, México, 2000.
24. Staindl O. Tissue adhesion with highly concentrated human fibrinogen in otolaryngology. Ann Otol 1979; 88: 413-8.
Agradecimientos
El autor de este estudio gradece y Cuello del Hospital Juárez de México, por su valiosa asesoría en la realización del presente trabajo; al QBP Conrado Medina Campos, asistente de la Jefatura de Banco de Sangre del Hospital Juárez de México por su y al Dr. César Germán Mondragón Galindo, Jefe del Servicio de Banco de Sangre de ese hospital por las la colaboración del Dr. Jerry Sandoval Serrano, sobre el uso y la preparación de adhesivos de fibrina.
